Wypróbuj PMC Labs i powiedz nam, co myślisz. Dowiedz się więcej .

COVAX-19Ⓡ Szczepionka: Całkowicie blokuje przenoszenie wirusa na osoby nieuodpornione
Vivek P. Chavda
aDepartment of Pharmaceutics and Pharmaceutical Technology, L M College of Pharmacy, Ahmedabad - 380009, Gujarat, India
Lalitkumar K. Vora
bSchool of Pharmacy, Queen's University Belfast, 97 Lisburn Road, BT9 7BL, UK
Disha R. Vihol
cPharmacy Section, L.M. College of Pharmacy, Ahmedabad - 380058, Gujarat, India
Powiązane dane
Abstrakcyjny
Różne platformy szczepionek są nastawione na opracowanie szczepionki przeciw COVID-19 w celu wytwarzania immunogenów w komórkach. Aby zaprojektować szczepionkę przeciw COVID-19 opartą na rekombinowanym białku, firma Vaxine pty Ltd wykorzystała modele komputerowe białka kolczastego i jego ludzkiego receptora, ACE2, w celu zidentyfikowania, w jaki sposób wirus infekuje ludzkie komórki. Na tej podstawie syntetyzuje się szczepionkę COVAX-19Ⓡ. Zmniejsza nie tylko chorobę COVID-19, ale także blokuje wydalanie i przenoszenie wirusa. Naukowcy są optymistyczni, że ta kandydatka na szczepionkę może wkrótce być dostępna klinicznie, przy wystarczającej skuteczności szczepionki przy znacznym ograniczeniu skutków ubocznych związanych ze szczepieniem.
1. Tło
Obecnie świat boryka się z pandemią SARS-CoV-2, a szczepionka jest dominującą opcją walki z nią. Około 119 kandydatów na szczepionki jest w trakcie opracowywania, a 15 szczepionek zostało zatwierdzonych na COVID-19. Istnieje rosnące zapotrzebowanie na nowszych, bezpiecznych i skutecznych kandydatów, ponieważ obecnie stosowane szczepionki okazały się nieskuteczne przeciwko nowym wariantom szczepu wirusa zdominowanego w różnych częściach świata. W sumie zatwierdzono 20 kandydatów na szczepionki do stosowania w sytuacjach awaryjnych, podczas gdy 131 kandydatów na szczepionki jest w trakcie opracowywania, a 383 trwają badania kliniczne.
2. COVAX-19Ⓡ Szczepionka
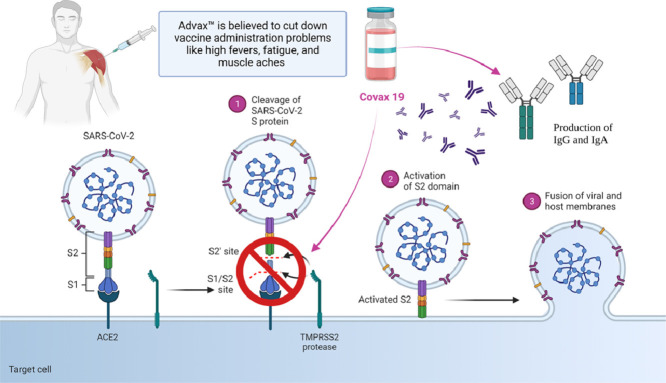
Ze względu na EUA (Emergency Use Authorization), długoterminowe dane dotyczące bezpieczeństwa i skuteczności szczepionek nie są dostępne i istnieje potencjalne ryzyko wybuchu epidemii ( Tabela 1 ). Poza tym, dostępne obecnie szczepionki nie dorównują leczeniu szybko mutującemu wirusowi covid. Dodatkowo zapewniane przez nich szczepienia trwają nie dłużej niż rok. Szczepionki nie mogą powstrzymać przenoszenia choroby, co prowadzi do powszechnych zaburzeń zdrowotnych, społecznych i ekonomicznych ( Li i wsp., 2020 ). Aby przezwyciężyć te problemy, profesor Nikolai Petrovsky z Flinders University i dyrektor ds. badań w Vaxine Pty Ltd z Adelaide w Australii Południowej opracował nową syntetyczną szczepionkę o nazwie COVAX-19Ⓡ. Składa się z nieszkodliwego, rekombinowanego białka wypustkowego SARS-CoV-2 na bazie komórek owadzich w połączeniu z opatentowanym przez Vaxine niezapalnym Advax™, adiuwantem polisacharydowym pochodzącym z delta inuliny. Odporność na SARS-CoV-2 wynika z wytwarzania neutralizujących przeciwciał i limfocytów T, które zapobiegają przyłączaniu się wirusa do ludzkiego receptora enzymu konwertującego angiotensynę 2 (ACE2) w nabłonku oddechowym ( Rys. 1 ) ( Vaxine Pty Ltd 2020 ).
Tabela 1
Komercjalizowane kandydaci na szczepionki przeciwko COVID-19 i ich pułapkom.
| Platforma szczepionek | Imię i nazwisko kandydata na szczepionkę | Nowator | Ugrupowanie docelowe | Pułapki | Bibliografia |
| Szczepionka oparta na mRNA | mRNA-1273 | Nowoczesne, USA | mRNA modyfikowany nukleozydami (modRNA) kodujący białko wypustek SARS-CoV-2 | Ograniczona skuteczność wobec wariantu beta i delta i wymaga dawki przypominającej. Reakcje anafilaktyczne zgłaszano również w 2,5% przypadków. Zapalenie przykrycia serca lub osierdzia. | ( Shimabukuro i in., 2021 ) |
| BNT162b2 (Tozinameran, Comirnaty) | Pfizer/BioNTech, USA i Niemcy | mRNA modyfikowany nukleozydami (modRNA) kodujący zmutowaną formę pełnej długości białka wypustkowego SARS-CoV-2 | Wymaga przechowywania w ultraniskiej temperaturze. Ograniczona skuteczność przeciwko odmianom beta i delta oraz potrzebna dawka przypominająca. Zgłoszono działania niepożądane związane ze szczepieniem. | ( Polack i in., 2020 ) | |
| TAK-919 | Takeda, Japonia | mRNA-1273.351, który może być użyty jako zastrzyk przypominający przeciwko wariantowi Beta | Ograniczona skuteczność wobec wariantu delta i wymaga dawki przypominającej. Zgłoszono działania niepożądane związane ze szczepieniem. | ( aktualizacja szczepionki Moderna 2021 ) | |
| Szczepionka podjednostkowa białkowa | ZF2001 (RBD-Dimer) | Anhui Zhifei Longcom, Chiny | Podjednostka białkowa z adiuwantem zawierająca domenę wiążącą receptor CoV (RBD) | Ograniczona skuteczność i wymaga dawki przypominającej nawet po 2 dawkach. | ( Yang i in., 2021 ) |
| EpiVacCorona | Fundacja Badań i Innowacji Biomedycznych w Kobe (FBRI), Japonia | Posiada trzy syntetyczne peptydy wirusowe (jeden kolec, jedno białko N i jeden peptyd bakteryjny), które są sprzężone z dużym białkiem nośnikowym | Ograniczona skuteczność i wymaga dawki przypominającej nawet po 2 dawkach. | ( Dobrovidova, 2021 ) | |
| Szczepionka oparta na wektorach adenowirusowych | Covishield | Surowica Instytut Indii | wektor ChAdOx1 kodują białka wirusowego kolca | Udokumentowano wiele doniesień o poważnych reakcjach alergicznych na te szczepionki. | ( Mohammad S Razai i Osama, 2021 ) |
| Vaxzevria (AZD1222) | Oksford/AstraZeneca, Wielka Brytania | ChAdOx1 wektor kodują białka wirusowego kolca | 234 doniesienia o poważnych reakcjach alergicznych na szczepionki AstraZeneca. Po podaniu szczepionki Oxford–AstraZeneca zgłoszono 30 przypadków anafilaksji | ( Mohammad S Razai i Osama, 2021 , Shimabukuro i in., 2021 ) | |
| Ad26COVS1, JNJ-78436735 | Janssen (Johnson & Johnson), USA | Wektor Ad26 koduje białko wirusowego kolca | Rzadkie zaburzenia krzepnięcia krwi po porodzie i stosunkowo mniej skuteczne | ( Viswanath, 2021 ) | |
| Gam-COVID-Vac | Gamaleja: Sputnik V, Rosja | Wektor Ad26 koduje białko wirusowych kolców i dawkę przypominającą z wektorem Ad5 kodującym białko wirusowe kolce | Wymaga przechowywania w stanie zamrożonym, stosunkowo mniej skuteczny i potrzebne są wielokrotne dawki. | ( Logunov i in., 2021 ) | |
| Ad5-nCoV | CanSino, Chiny | Wektor Ad5 koduje białko wirusowego kolca | |||
| Inaktywowana Szczepionka | CoronaVac | Sinovac Pharma Inc., Chiny | Inaktywowany cały wirus tj. SARS-CoV-2 | Wymaga przechowywania w stanie zamrożonym, stosunkowo mniej skuteczny i wymagane jest wielokrotne dozowanie. | ( Han i in., 2021 ) |
| BBIBP-CorV | Sinopharma, Pekin, Chiny | Wymaga dawki przypominającej i zgłoszonych skutków ubocznych związanych ze szczepieniem. | ( Al Kaabi i in., 2021 ) | ||
| WIBP-CorV | Sinopharma, Wuhan, Chiny | Requires booster dose and vaccination-related side effects reported. | ( Al Kaabi i in., 2021 ) | ||
| SARS-CoV-2 Vaccine (Vero Cells) | Minhai Biotechnology Co., Beijing, China | Requires booster dose and vaccination-related side effects reported. | (Zhang et al., 2021) | ||
| QazVac | Research Institute for Biological Safety Problems in Kazakhstan | Requires booster dose and vaccination-related side effects reported. | (Batyrov, 2021) | ||
| KoviVac | Chumakov Center, Russia | Requires booster dose and vaccination-related side effects reported. Less effective against the variants of SARS-CoV-2. | (Mir, 2021) | ||
| Covaxin | Bharat Biotech, India | Neurological problems reported, requires booster dose and vaccination-related side effects reported. Less effective against the variants of SARS-CoV-2. | (Thiagarajan, 2021) | ||
Ponadto uważa się, że zastosowanie adiuwantu przeciwzapalnego, Advax™ (delta-inulina klasy GMP), zmniejsza problemy związane z podawaniem szczepionki, takie jak wysoka gorączka, zmęczenie i bóle mięśni, które są powszechnie obserwowane w obecnie zatwierdzonej szczepionce ( Petrovsky , 2020 ). Zespół zidentyfikował i potwierdził rolę białka szczytowego SARS-CoV-2 za pomocą Etaluma Luma Scope LS620 dostarczonego przez AXT Pty Ltd ( Chai, 2021 ). Aby określić cele, zespół wykorzystał superkomputer w chmurze Oracle i sztuczną inteligencję (AI) do opracowania COVAX-19Ⓡ w zaledwie pięć tygodni, co zwykle zajmuje około 15 lat.
Wraz z celem dla COVAX-19Ⓡ odkryli również około 80 możliwych celów przeciwko SARS-CoV-2 i udostępnili je światu do badań ( Piplani i in., 2020 ). W celu prowadzenia rozwoju produktów i procesów, programów badań klinicznych i zwiększenia skali handlowej na rynkach australijskim i azjatyckim, firma podpisała protokół ustaleń z wysoce doświadczoną firmą produkującą GMP Medytox biopharma z Korei Południowej ( partner Vaxine i Medytox w Covid- 19 rozwój szczepionek 2020 ). Ponadto APC, irlandzka farmaceutyczna firma badawcza, która projektuje, rozwija i dystrybuuje opatentowane technologie platform inżynierskich w celu zminimalizowania czasu, kosztów i ryzyka związanego z opracowywaniem leków, współpracowała z Vaxine w celu przyspieszenia rozwoju i marketingu COVAX-19Ⓡ ( Taylor, 2021 ).
COVAX-19Ⓡ został przeniesiony do fazy I badania klinicznego po uzyskaniu długotrwałej ochrony z doskonałymi wynikami bezpieczeństwa i tolerancji z badań przedklinicznych na myszach, fretkach i małpach, które są prowadzone we współpracy z University of Georgia, USA ( Petrovsky, 2020 ). Badanie fazy I zostało również przeprowadzone niezależnie przez zespół badań klinicznych PARC, grupę badawczą z University of Adelaide w Royal Adelaide Hospital, w której uczestniczyło 40 zdrowych uczestników w wieku od 18 do 65 lat ( {"type":"próba kliniczna" ,"attrs":{"text":"NCT04453852","term_id":"NCT04453852"}} NCT04453852 ). Uczestnicy zostali losowo przydzieleni w stosunku 3:1 do otrzymania dwóch dawek domięśniowych w odstępie trzech tygodni albo aktywnej szczepionki w dawce 25 µg białka kolczastego plus 15 mg Advax™ i 0,15 mg CpG55.2 (30 uczestników) albo placebo w soli fizjologicznej (10 uczestników) ( Vaxine Pty Ltd 2020 ). Badanie fazy II trwa w Iranie w Espinas Palace Hotel w Teheranie, z udziałem 400 uczestników (18 i 65 lat) w celu oceny immunogenności i bezpieczeństwa (IRCT20150303021315N23), które jest dwuramiennym, podwójnie zaślepionym, kontrolowanym placebo badaniem . Wyniki nie zostały jeszcze ogłoszone w szczegółowej formie, ale zespół zapewnił, że szczepionka jest bardzo bezpieczna i tolerowana, a także nie przenosi się Covid-19 między osobnikami. Sugerują również, że COVAX-19Ⓡ zapewni skuteczną odporność stada. Według ostatnich wiadomości firmy, szczepionka COVAX-19Ⓡ wejdzie w fazę II i III badań klinicznych z umową o współpracy z Iranem. A jeśli te badania zakończą się sukcesem, szczepionka zostanie wprowadzona w Iranie pod marką „SpikoGenⓇ” firmy CinnaGen ( SpikogenⓇ, 2021 ). W porównaniu z innymi zatwierdzonymi w sytuacjach awaryjnych kandydatami na szczepionki przeciw zakażeniu SARS-COV-2, COVAX-19Ⓡ prowadzi do mniejszych skutków ubocznych związanych z podaniem szczepionki ze względu na przeciwzapalny adiuwant obecny w preparacie szczepionki. Przeciwzapalny adiuwant i syntetyczne wirusowe elementy białkowe w preparacie szczepionki również wskazują na lepszy margines bezpieczeństwa i tolerancję tego kandydata na szczepionkę. Co więcej, Nikołaj Pietrowski spodziewa się, że szczepionka będzie skuteczna wobec nowych zmutowanych szczepów RPA (wariant Beta), Brazylii (wariant Gamma) i Indii (wariant Delta), z odpornością trwającą co najmniej dwa lata.
Oświadczenie o wkładzie autorskim CRediT
Vivek P Chavda przygotował szkielet rękopisu, napisał oryginalny szkic rękopisu z Disha Vihol. Lalitkumar K Vora i Vivek P Chavda dopracowali projekt, a wszyscy autorzy zatwierdzili przedłożoną wersję. Figurka jest tworzona za pomocą BioRender.com
Deklaracja Konkurencyjnego Interesu
Autorzy deklarują, że nie znają sprzecznych interesów finansowych ani osobistych powiązań, które mogłyby mieć wpływ na pracę opisaną w tym artykule.
Bibliografia
- Al Kaabi N., Zhang Y., Xia S., Yang Y., Al Qahtani M.M., Abdulrazzaq N., Al Nusair M., Hassany M., Jawad J.S., Abdalla J., Hussein S.E., Al Mazrouei S.K., Al Karam M., Li X., Yang X., Wang W., Lai B., Chen W., Huang S., Wang Q., Yang T., Liu Y., Ma R., Hussain Z.M., Khan T., Saifuddin Fasihuddin M., You W., Xie Z., Zhao Y., Jiang Z., Zhao G., Zhang Y., Mahmoud S., ElTantawy I., Xiao P., Koshy A., Zaher W.A., Wang H., Duan K., Pan A., Yang X. Effect of 2 Inactivated SARS-CoV-2 Vaccines on Symptomatic COVID-19 Infection in Adults: A Randomized Clinical Trial. JAMA. 2021 doi: 10.1001/jama.2021.8565. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Batyrov Azamat. 2021. Kazakhstan Launches Production of First Homegrown Vaccine. ‘QazVac,’ (n.d.) April 25. https://caspiannews.com/news-detail/kazakhstan-launches-production-of-first-homegrown-vaccine-qazvac-2021-4-25-0/ (accessed June 18, 2021) [Google Scholar]
- Chai Cameron S. AXT Assists Vaxine in the Search for a COVID-19 Vaccine. Etradewire. 2021 https://etradewire.com/news/axt-assists-vaxine-in-the-search-for-covid-19-vaccine (accessed May 22, 2021) [Google Scholar]
- Dobrovidova O. Latest Russian vaccine comes with a big dose of mystery. Science. 2021;372:116–117. doi: 10.1126/science.372.6538.116. [PubMed] [CrossRef] [Google Scholar]
- B. Han, Y. Song, C. Li, W. Yang, Q. Ma, Z. Jiang, M. Li, X. Lian, W. Jiao, L. Wang, Q. Shu, Z. Wu, Y. Zhao, Q. Li, Q. Gao, Safety, tolerability, and immunogenicity of an inactivated SARS-CoV-2 vaccine (CoronaVac) in healthy children and adolescents: a double-blind, randomised, controlled, phase 1/2 clinical trial, Lancet Infect. Dis. (2021). doi:10.1016/S1473-3099(21)00319-4. [PMC free article] [PubMed] [CrossRef]
- Li Y., Tenchov R., Smoot J., Liu C., Watkins S., Zhou Q. A Comprehensive Review of the Global Efforts on COVID-19 Vaccine Development. ACS Cent. Sci. 2021;7:512–533. doi: 10.1021/acscentsci.1c00120. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Logunov D.Y., Dolzhikova I.V, Shcheblyakov D.V, Tukhvatulin A.I., Zubkova O.V, Dzharullaeva A.S., Kovyrshina A.V, Lubenets N.L., Grousova D.M., Erokhova A.S., Botikov A.G., Izhaeva F.M., Popova O., Ozharovskaya T.A., Esmagambetov I.B., Favorskaya I.A., Zrelkin D.I., Voronina D.V, Shcherbinin D.N., Semikhin A.S., Simakova Y.V, Tokarskaya E.A., Egorova D.A., Shmarov M.M., Nikitenko N.A., Gushchin V.A., Smolyarchuk E.A., Zyryanov S.K., Borisevich S.V, Naroditsky B.S., Gintsburg A.L. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. Lancet (London, England) 2021;397:671–681. doi: 10.1016/S0140-6736(21)00234-8. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Mir Russkiy. 2021. Developer: Kovivac Is Effective Against All Covid-19 Mutations. https://russkiymir.ru/en/news/287084/ (accessed June 16, 2021) [Google Scholar]
- Moderna’s vaccine update, (2021) January 25th, 2021. https://investors.modernatx.com/static-files/1f770088-5909-457b-af99-7ff2454ba28a (accessed June 18, 2021).
- Mohammad S Razai A.M., Osama Tasnime. Covid-19 vaccine adverse events: balancing monitoring with confidence in vaccines. BMJ Opin. 2021 [Google Scholar]
- Petrovsky Nikolai. 2020. Vaxine and University of Georgia Completes First Stage of COVID-19 Ferret Challenge Studies, Einpresswire. https://vaxine.net/vaxine-and-university-of-georgia-complete-first-stage-of-covid-19-ferret-challenge-studies/ (accessed May 22, 2021) [Google Scholar]
- Piplani S., Singh P., Petrovsky N., Winkler D.A. 2020. Computational screening of repurposed drugs and natural products against SARS-Cov-2 main protease (Mpro) as potential COVID-19 therapies. http://arxiv.org/abs/2009.00744 (accessed May 22, 2021) [Google Scholar]
- Polack F.P., Thomas S.J., Kitchin N., Absalon J., Gurtman A., Lockhart S., Perez J.L., Pérez Marc G., Moreira E.D., Zerbini C., Bailey R., Swanson K.A., Roychoudhury S., Koury K., Li P., Kalina W.V, Cooper D., Frenck R.W., Hammitt L.L., Türeci Ö., Nell H., Schaefer A., Ünal S., Tresnan D.B., Mather S., Dormitzer P.R., Şahin U., Jansen K.U., Gruber W.C. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. N. Engl. J. Med. 2020;383:2603–2615. doi: 10.1056/NEJMoa2034577. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Shimabukuro, et al. Allergic Reactions Including Anaphylaxis After Receipt of the First Dose of Moderna COVID-19 Vaccine - United States. December 21, 2020-January 10. MMWR. Morb. Mortal. Wkly. Rep. 2021;70:125–129. doi: 10.15585/mmwr.mm7004e1. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Shimabukuro T.T., Cole M., Su J.R. Reports of Anaphylaxis after Receipt of mRNA COVID-19 Vaccines in the US-December 14, 2020-January 18, 2021. JAMA - J. Am. Med. Assoc. 2021;325:1101–1102. doi: 10.1001/jama.2021.1967. [PubMed] [CrossRef] [Google Scholar]
- SpikogenⓇ A Joint. 2021. Venture Between Vaxine And Cinnagen.https://vaxine.net/spikogen-a-joint-venture-between-vaxine-and-cinnagen/ (accessed May 22, 2021) [Google Scholar]
- Taylor Charlie. 2021. Pharma research firm APC partners to develop Covid-19 vaccine. https://www.irishtimes.com/business/health-pharma/pharma-research-firm-apc-partners-to-develop-covid-19-vaccine-1.4275430 (accessed May 22, 2021) [Google Scholar]
- Thiagarajan K. What do we know about India's Covaxin vaccine? BMJ. 2021;373:n997. doi: 10.1136/bmj.n997. [PubMed] [CrossRef] [Google Scholar]
- Vaxine and Medytox partner on Covid-19 vaccine development Pharm. Technol. 2020 https://www.pharmaceutical-technology.com/news/vaxine-medytox-covid-19-vaccine/ (accessed May 22, 2021) [Google Scholar]
- Vaxine Pty Ltd . ClinicalTrials.gov Identifier: NCT04453852; 2020. Phase 1 Cilinical trials on Monovalent Recombinant COVID19 Vaccine (COVAX19) https://clinicaltrials.gov/ct2/show/{"type":"clinical-trial","attrs":{"text":"NCT04453852","term_id":"NCT04453852"}}NCT04453852 (accessed May 22, 2021) [Google Scholar]
- Viswanath PILLA. Money Control; 2021. Rare clot incidents linked to J&J, AstraZeneca COVID-19 vaccines bring adenovirus vector platform under scanner.https://www.moneycontrol.com/news/business/companies/rare-clot-incidents-linked-to-jj-astrazeneca-covid-19-vaccines-bring-adenovirus-vector-platform-under-scanner-6774801.html (accessed May 14, 2021) [Google Scholar]
- Yang S., Li Y., Dai L., Wang J., He P., Li C., Fang X., Wang C., Zhao X., Huang E., Wu C., Zhong Z., Wang F., Duan X., Tian S., Wu L., Liu Y., Luo Y., Chen Z., Li F., Li J., Yu X., Ren H., Liu L., Meng S., Yan J., Hu Z., Gao L., Gao G.F. Safety and immunogenicity of a recombinant tandem-repeat dimeric RBD-based protein subunit vaccine (ZF2001) against COVID-19 in adults: two randomised, double-blind, placebo-controlled, phase 1 and 2 trials. Lancet Infect. Dis. 2021 doi: 10.1016/S1473-3099(21)00127-4. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Y. Zhang, G. Zeng, H. Pan, C. Li, Y. Hu, K. Chu, W. Han, Z. Chen, R. Tang, W. Yin, X. Chen, Y. Hu, X. Liu, C. Jiang, J. Li, M. Yang, Y. Song, X. Wang, Q. Gao, F. Zhu, Safety, tolerability, and immunogenicity of an inactivated SARS-CoV-2 vaccine in healthy adults aged 18–59 years: a randomised, double-blind, placebo-controlled, phase 1/2 clinical trial, Lancet Infect. Dis. 21 (2021) 181–192. doi:10.1016/S1473-3099(20)30843-4. [PMC free article] [PubMed] [CrossRef]
Formaty:
- Artykuł |
- PubReader |
- ePub (beta) |
- PDF (722K) |
- Cytować
-
Szczepionka COVAX-19Ⓡ: Całkowicie blokuje przenoszenie wirusa na osoby nieuodpornione... COVAX-19Ⓡ Szczepionka: Całkowicie blokuje przenoszenie wirusa na osoby nieuodpornioneZbiórka ratunkowa w zakresie zdrowia publicznego Elsevier. 2021 gru; 1(1)100004
Your browsing activity is empty.
Activity recording is turned off.
Zobacz więcej...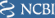
 Facebook
Facebook
 Świergot
Świergot
 Google+
Google+